Las enzimas son máquinas moleculares que llevan a cabo las reacciones químicas que sostienen toda forma de vida. Este fenómeno ha despertado el interés de numerosos científicos, quienes se cuestionan sobre su potencial para resolver problemas contemporáneos. Un ejemplo claro de su importancia se encuentra en el funcionamiento del sistema muscular humano. Cuando se libera acetilcolina, esta molécula desencadena la contracción de las células musculares. Sin embargo, si la acetilcolina persiste demasiado tiempo, puede provocar parálisis, poniendo en riesgo la vida. Aquí es donde entra en juego la enzima acetilcolinesterasa, la cual descompone miles de moléculas de acetilcolina por segundo, asegurando la correcta contracción muscular y evitando situaciones de emergencia. Sin esta enzima, la descomposición de la acetilcolina podría tardar un mes, lo que representa una diferencia de velocidad de aproximadamente 10 mil millones de veces.
La capacidad de las enzimas para actuar con rapidez ha llevado a los investigadores a preguntarse si podrían diseñar nuevas enzimas capaces de abordar desafíos globales, como la degradación de plásticos, la captura de dióxido de carbono o el tratamiento de células cancerosas. Sin embargo, el diseño de enzimas resulta ser un proceso extremadamente complicado, comparable a ensamblar un set de Lego a escala atómica sin instrucciones claras. Recientes investigaciones sugieren que el aprendizaje automático puede actuar como un arquitecto en este complejo proceso, facilitando la construcción de estas estructuras moleculares.
La complejidad del diseño enzimático
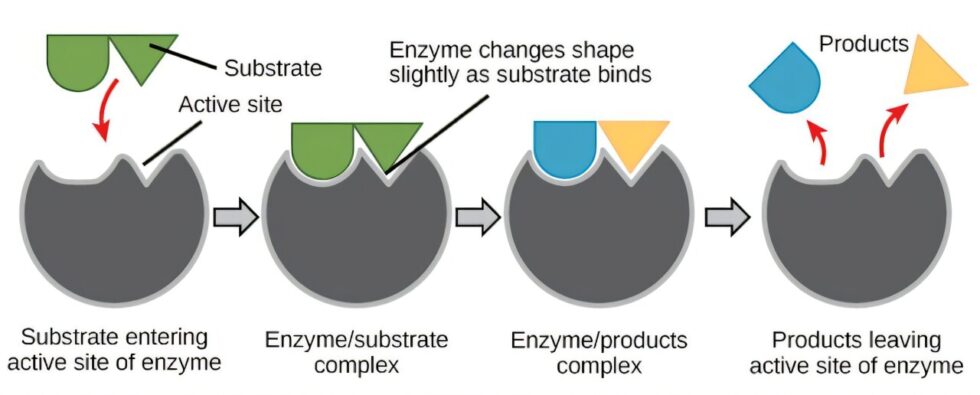
Las enzimas son proteínas compuestas por largas cadenas de aminoácidos que se pliegan en estructuras específicas. La función de una enzima está intrínsecamente relacionada con su forma; así como una cuchara está diseñada para contener líquido, cada enzima tiene una configuración particular que le permite interactuar con su molécula objetivo. Esta interacción se produce en una región conocida como el sitio activo, donde la enzima orienta a los aminoácidos de manera precisa para facilitar la reacción química.
A lo largo de las últimas décadas, los científicos han intentado diseñar enzimas nuevas que puedan sintetizar moléculas, materiales o terapias. Sin embargo, hacerlo de manera que estas enzimas imiten la velocidad y eficiencia de las enzimas naturales es un reto monumental. Las enzimas tienen formas complejas e irregulares, y cada aminoácido debe ser colocado con una precisión extrema. Las diferencias en la estructura de las enzimas pueden determinar su eficacia, y pequeños errores pueden resultar en una disminución drástica en su actividad.
Las estrategias iniciales se centraron en modificar secuencias de aminoácidos de enzimas existentes para mejorar su velocidad o estabilidad. Sin embargo, estas modificaciones a menudo no lograban aumentar la velocidad de reacción. En su lugar, la evolución dirigida, que implica la alteración aleatoria de secuencias de aminoácidos, ha demostrado ser un método más efectivo. A pesar de su éxito, este enfoque es intensivo en recursos y tiempo, ya que se deben evaluar múltiples mutantes para encontrar uno que funcione adecuadamente.
Una de las limitaciones de estos métodos es su dependencia de las enzimas naturales. Al restringir el diseño a las formas de proteínas ya existentes, se limita el tipo de química que se puede facilitar. La búsqueda de soluciones innovadoras ha llevado a los científicos a explorar el uso de la computación en el diseño de enzimas.
El papel de la inteligencia artificial en el diseño de enzimas
Los primeros intentos de diseñar enzimas computacionalmente todavía se basaban en estructuras de enzimas naturales. Sin embargo, avances recientes en aprendizaje profundo han transformado este campo. Herramientas de inteligencia artificial, como el modelo RFdiffusion, permiten generar estructuras enzimáticas que se adaptan perfectamente a los sitios activos sin depender de las proteínas nativas. Este proceso se asemeja a solicitar a un programa de inteligencia artificial la creación de un relato completo a partir de una línea guía.
En estudios recientes, los investigadores han utilizado estas herramientas para diseñar enzimas específicas, como las hidrolasas de serina, que tienen aplicaciones prometedoras en medicina y reciclaje de plásticos. Al evaluar las enzimas diseñadas, se ha comprobado que muchas de ellas pueden catalizar reacciones de descomposición de moléculas de manera más eficaz que las enzimas previamente diseñadas. Además, técnicas como la cristalografía de rayos X han confirmado la precisión de las estructuras generadas por computadora.
Estos avances subrayan el papel crucial que la inteligencia artificial puede desempeñar en la resolución de problemas complejos del mundo moderno, evidenciando cómo la tecnología puede facilitar el acceso al diseño de enzimas y maximizar su potencial para abordar desafíos globales.







