En los últimos dos años, la investigación genética ha avanzado a pasos agigantados, vinculando miles de variantes del ADN con diversas enfermedades y características humanas. Sin embargo, el tratamiento de estas enfermedades a través de la corrección de los efectos de dichas variantes se ha visto obstaculizado por la falta de herramientas moleculares precisas. Un equipo de investigadores del Instituto Broad del MIT y Harvard, junto con el Hospital General de Massachusetts y la Universidad de Harvard, ha desarrollado un enfoque innovador para abordar este desafío.
Los científicos han creado una colección diversa de compuestos moleculares que pueden ser utilizados para identificar aquellos que afectan a las variantes genéticas relacionadas con enfermedades de nuevas maneras. Gracias a métodos químicos innovadores, esta biblioteca incluye más de 3 millones de compuestos diseñados para unir dos proteínas, utilizando una de ellas como un escudo para estabilizar la otra y revertir sus efectos perjudiciales relacionados con enfermedades.
Un nuevo enfoque en la química médica
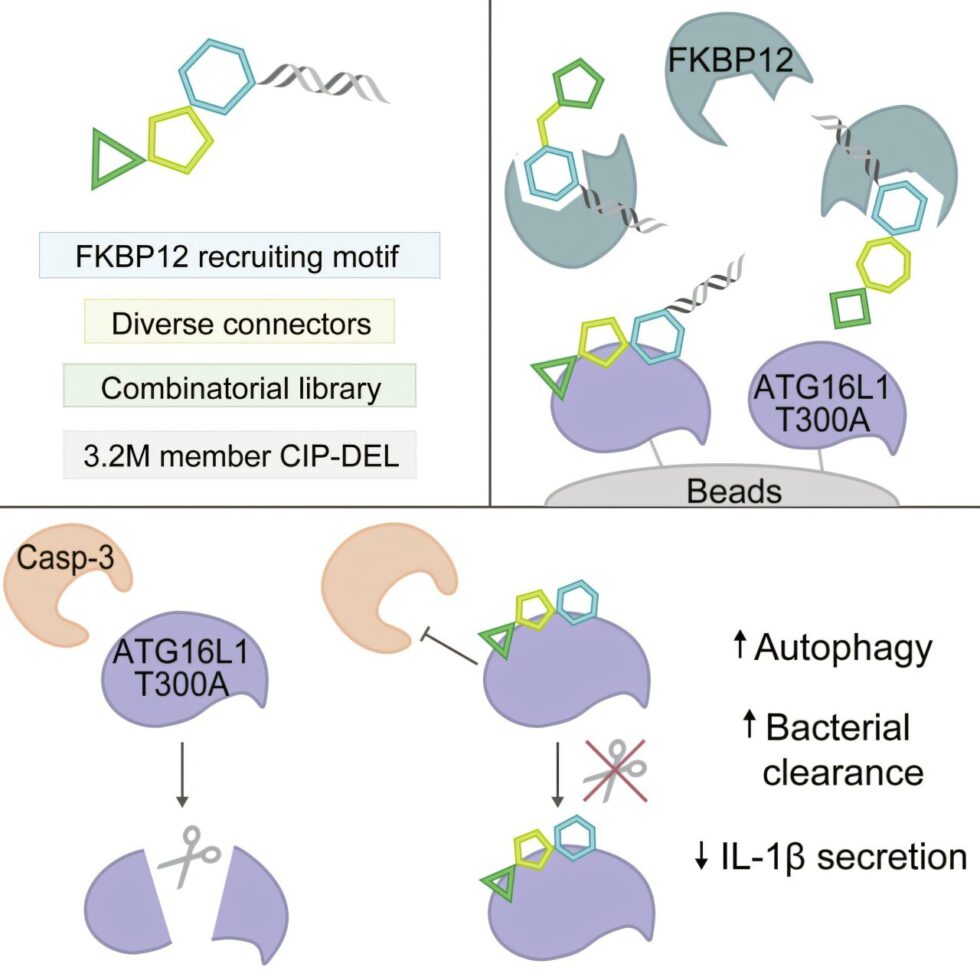
En su búsqueda de compuestos que alteren proteínas relacionadas con enfermedades, los investigadores han desarrollado lo que se conoce como inductor químico de proximidad (CIP), que incluye compuestos bifuncionales y «pegamentos» moleculares. Estos compuestos permiten que dos proteínas en la célula, que normalmente no interaccionarían, se unan—una proteína «objetivo» (a menudo alterada por la enfermedad) y una proteína «presentadora» que influye en la primera.
Tradicionalmente, la mayoría de las bibliotecas de CIP se han centrado en inducir la degradación de la proteína disfuncional mediante el uso de la maquinaria de eliminación de desechos de la célula, lo que reduce sus efectos nocivos. Sin embargo, en el nuevo estudio, los investigadores se han enfocado en construir una biblioteca de CIPs que realicen funciones distintas a la degradación de la proteína objetivo. Para ello, eligieron como proteína presentadora a FKBP12, un componente bien estudiado que abunda en las células humanas.
El equipo postuló que, al ser activada por un CIP, FKBP12 podría actuar como un escudo para proteger a una proteína objetivo de las enzimas que normalmente la descomponen, estabilizándola. Este enfoque podría ser suficiente para restaurar la función normal de algunas proteínas relacionadas con enfermedades como una forma de tratamiento.
Mediante la creación de una biblioteca de compuestos que cubriera un amplio «espacio químico», los investigadores generaron una biblioteca de ADN codificado (CIP-DEL) con más de 3 millones de compuestos únicos que reclutan FKBP12. En un experimento, identificaron un compuesto que interactuó con una variante genética asociada con el riesgo de enfermedad de Crohn, estabilizando la proteína alterada y restaurando procesos celulares vitales.
El director del programa de inmunología del Instituto Broad, Ramnik Xavier, subrayó el potencial de estas nuevas estrategias químicas y su integración con la genética humana para desarrollar tratamientos innovadores. Los investigadores planean avanzar en el desarrollo de un compuesto que funcione en modelos animales para explorar más oportunidades terapéuticas.
Este enfoque no solo abre nuevas vías para intervenir en enfermedades humanas, sino que también permite personalizar la biblioteca CIP-DEL para abordar variantes de enfermedades específicas, lo que podría resultar en tratamientos más efectivos y menos invasivos.