Un equipo de investigación internacional ha logrado un avance significativo en la comprensión de los mecanismos genéticos que permiten a las bacterias desarrollar resistencia a los antibióticos, un problema que representa una de las principales amenazas para la salud pública a nivel global.
Las bacterias cuentan con múltiples mecanismos de defensa que les ayudan a adquirir resistencia a los antibióticos. Uno de estos mecanismos implica el uso de plásmidos, pequeñas moléculas de ADN que poseen su propio genoma independiente y que son responsables de la resistencia a los medicamentos. Comprender el papel que desempeñan estos plásmidos en las bacterias podría abrir la puerta al desarrollo de una nueva generación de terapias que apunten a infecciones resistentes a los fármacos.
Investigadores del John Innes Center, en colaboración con expertos de Madrid, Nueva York y Birmingham, han utilizado un modelo de plásmido conocido como RK2, ampliamente empleado para el estudio de plásmidos clínicamente relevantes que transmiten resistencia antimicrobiana. El estudio, titulado «KorB switching from DNA-sliding clamp to repressor mediates long-range gene silencing in a multi-drug resistance plasmid,» ha sido publicado en Nature Microbiology.
El Mecanismo KorB-KorA
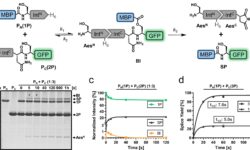
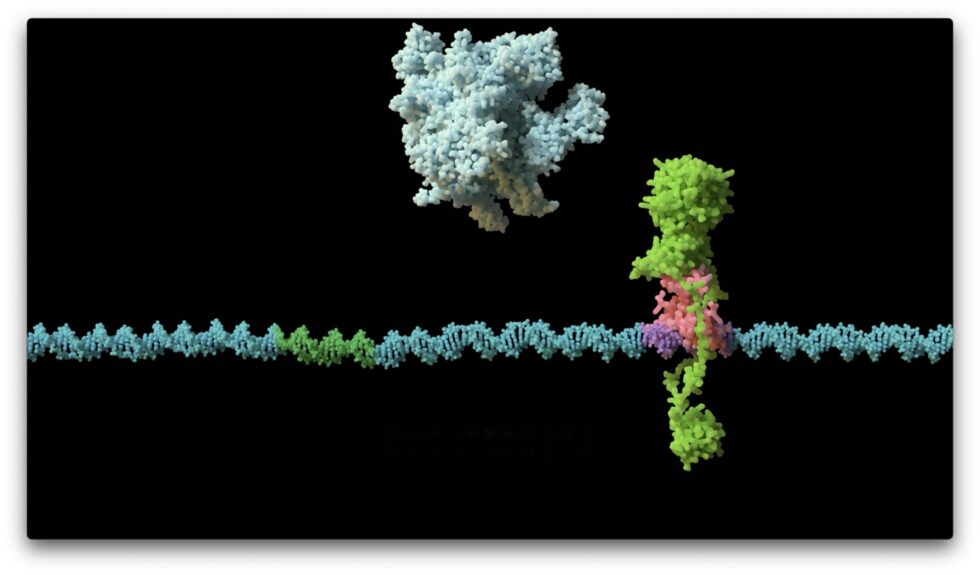
El enfoque inicial del equipo se centró en una molécula llamada KorB, esencial para la supervivencia de los plásmidos en sus hospedadores bacterianos. Aunque se conocía que esta proteína que se une al ADN desempeñaba un papel en el control de la expresión génica, su funcionamiento exacto no estaba claro. Mediante técnicas avanzadas de microscopía y cristalografía de proteínas, el equipo descubrió que KorB interactúa con otra molécula denominada KorA. Este sistema regulador KorB-KorA actúa como un mecanismo de represión de la expresión génica, donde KorB funciona como una abrazadera deslizante de ADN y KorA como una cerradura que mantiene a KorB en su lugar.
Juntos, estos componentes complejos desactivan la expresión génica para proteger al plásmido dentro de su hospedador bacteriano. Este nuevo mecanismo ofrece una perspectiva renovada sobre el silenciamiento génico a larga distancia en bacterias, permitiendo que elementos regulatorios como el complejo KorB-KorA interactúen con genes diana distantes, inhibiendo su actividad para favorecer la supervivencia del plásmido.
El Dr. Thomas McLean, primer autor del estudio y investigador postdoctoral en el John Innes Center, ha destacado que este descubrimiento es un triunfo de la ciencia impulsada por la curiosidad. Originalmente, el proyecto se centraba en KorB, pero un experimento realizado de manera casual y sin un objetivo definido llevó al equipo a descubrir la capacidad de KorA para fijar a KorB en el lugar correcto en el momento adecuado.
Este hallazgo representa un gran avance que ha cambiado drásticamente la dirección del proyecto. Según McLean, el estudio proporciona un nuevo paradigma para la regulación genética a larga distancia en bacterias y ofrece una diana para terapias novedosas que puedan desestabilizar plásmidos en sus hospedadores y re-sensibilizarlos a los antibióticos.
Este trabajo también resuelve un enigma que ha perdurado durante décadas en el campo de la microbiología, relacionado con cómo la crítica proteína KorB controla la activación y desactivación de los genes en el plásmido RK2 resistente a múltiples fármacos. La investigación se ampliará para incluir más plásmidos clínicamente relevantes y explorar más a fondo el mecanismo KorB-KorA, buscando comprender cómo se desensambla en el momento adecuado.
Más información:
KorB switching from DNA-sliding clamp to repressor mediates long-range gene silencing in a multi-drug resistance plasmid, Nature Microbiology (2025). DOI: 10.1038/s41564-024-01915-3