Un equipo de investigación de Helmholtz Munich y la Universidad Técnica de Múnich ha desarrollado un avanzado sistema de entrega que transporta herramientas de edición genética basadas en el sistema CRISPR/Cas9 a células vivas con una eficiencia significativamente mayor que antes. Esta tecnología, denominada ENVLPE, utiliza partículas similares a virus no infecciosos para corregir de manera precisa genes defectuosos; se ha demostrado su eficacia en modelos de ratones ciegos debido a una mutación genética.
Además, este sistema promete avanzar en la terapia del cáncer al permitir la manipulación genética precisa de células inmunitarias modificadas, lo que las haría más compatibles y, por tanto, accesibles para un mayor número de pacientes oncológicos. La investigación ha sido publicada en la revista Cell.
Superando los desafíos de entrega en la edición genética
Las técnicas modernas de edición del genoma, incluidas las basadas en CRISPR, poseen un gran potencial para tratar enfermedades genéticas. Sin embargo, la entrega confiable de estas herramientas moleculares a las células diana sigue siendo un desafío significativo. Según el Dr. Dong-Jiunn Jeffery Truong, autor principal del estudio y líder del grupo en el Instituto de Biomedicina Sintética de Helmholtz Munich, los sistemas de entrega anteriores, como los virus asociados a adenovirus (AAV) y las nanopartículas lipídicas (LNP), aunque valiosos, presentan limitaciones en cuanto a su eficiencia y la posibilidad de provocar reacciones inmunitarias.
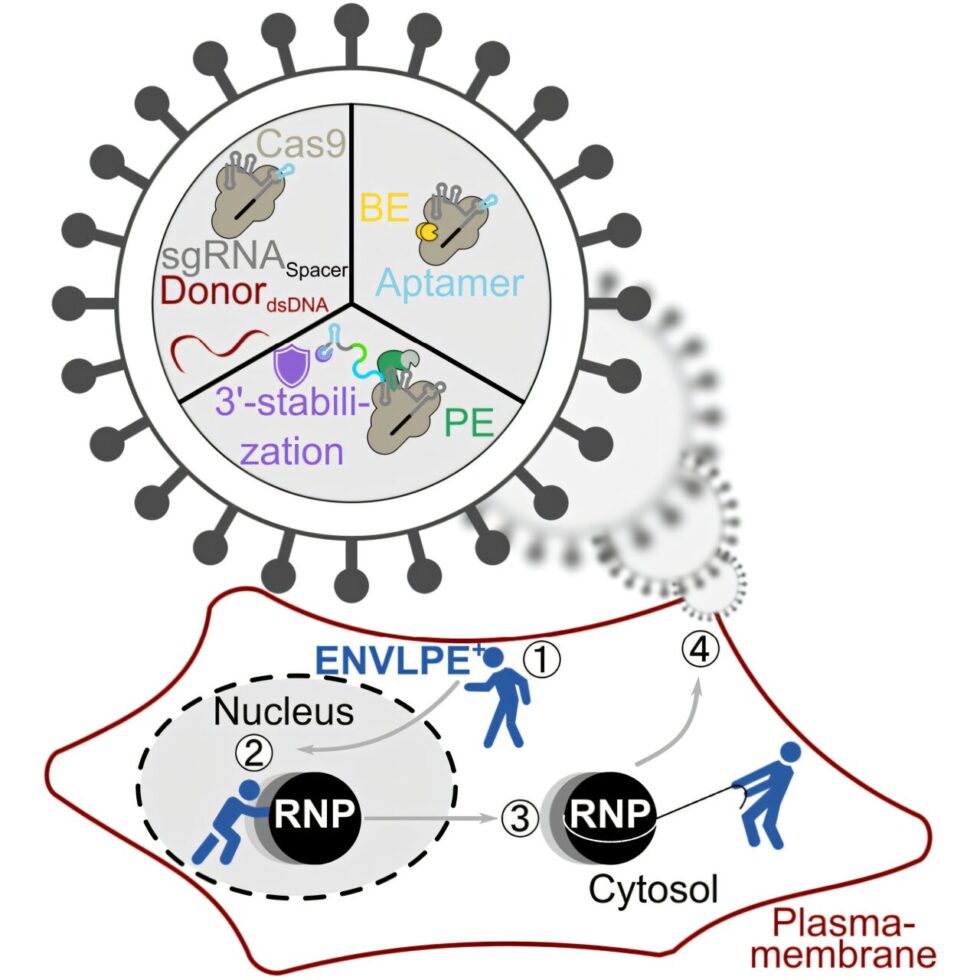
ENVLPE aborda directamente estos problemas, manteniendo un diseño modular que permite su compatibilidad con futuros avances en la edición genética. Este sistema se basa en caparazones derivados de virus modificados y no infecciosos, que actúan como transportadores para editores genéticos como los editores de bases o prime editors, herramientas especializadas de CRISPR que pueden cambiar químicamente bases de ADN individuales en el genoma.
Una de las innovaciones clave de ENVLPE es su capacidad para asegurar la correcta ensambladura de los editores genéticos, evitando el problema de los editores parcialmente ensamblados y no funcionales que limitaban la efectividad de la entrega en métodos anteriores. Además, incluye una capa molecular adicional que protege la parte más vulnerable del editor durante el transporte, lo que permite una entrega segura a las células diana donde se pueden realizar las modificaciones genéticas deseadas.
En colaboración con un equipo liderado por el Prof. Krzysztof Palczewski de la Universidad de California en Irvine, los científicos probaron el sistema ENVLPE en un modelo de ratón con ceguera hereditaria. Los ratones, que portan una mutación en el gen Rpe65, esencial para la producción de moléculas sensibles a la luz en la retina, recuperaron la respuesta a estímulos luminosos tras la inyección del sistema ENVLPE en el espacio subretiniano. Los resultados fueron sorprendentes, mostrando un potencial terapéutico real en un modelo animal.
Comparado con los sistemas establecidos, ENVLPE logró resultados significativamente mejores, requiriendo más de diez veces menos dosis para conseguir efectos similares. Con este desarrollo, el equipo busca construir una herramienta útil tanto para la investigación como para aplicaciones en el mundo real, resolviendo cuellos de botella críticos y logrando un empaquetamiento más eficiente.
ENVLPE también podría abrir nuevas posibilidades para las terapias de células T adoptivas, donde se modifican genéticamente células inmunitarias extraídas del paciente para que reconozcan y ataquen específicamente las células tumorales. En colaboración con el laboratorio de la Dra. Andrea Schmidts en el Hospital Universitario de TUM, los investigadores utilizaron ENVLPE para facilitar la eliminación de moléculas de superficie específicas que podrían desencadenar una respuesta inmunitaria al ser administradas a un receptor diferente del donante. Esto podría llevar al desarrollo de células T «universales» que no necesiten ser personalizadas para cada paciente, haciendo los tratamientos más accesibles y rentables.
Con la entrega de herramientas de edición genética más comunes lograda con éxito, el equipo ahora busca utilizar la diversidad que ofrece la naturaleza, junto con los recientes avances en el diseño de proteínas asistido por inteligencia artificial, para aumentar la precisión de la entrega al restringir el suministro de estas herramientas a tipos celulares o tejidos específicos. Para avanzar hacia la aplicación clínica del sistema ENVLPE, el equipo está buscando financiación a través de subvenciones de traducción y asociaciones en la industria farmacéutica, con el objetivo de optimizar la tecnología para diversas aplicaciones terapéuticas y, en última instancia, ponerla a disposición de los pacientes.